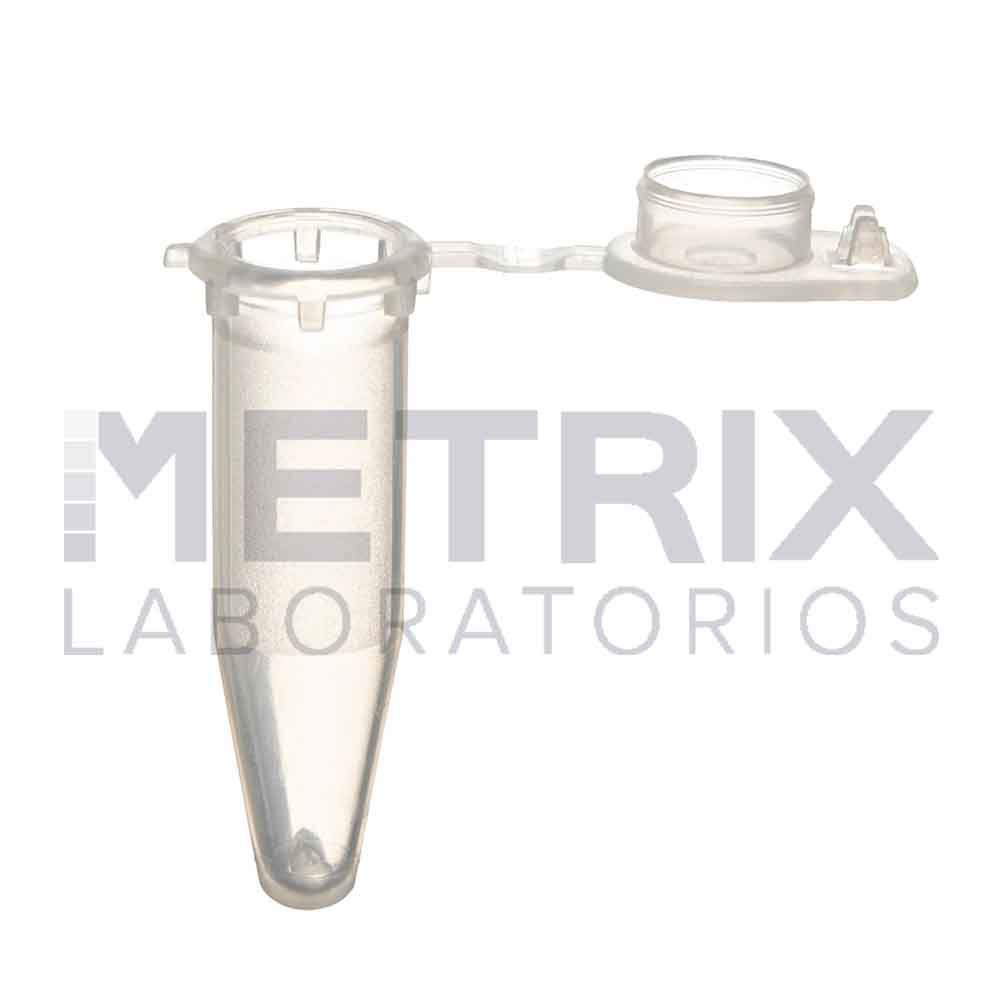
Metrix Laboratorios
Bienvenidos a Metrix Laboratorios
El científico que puso orden a toda la vida en la Tierra.
23 de mayo – Un antes y un después en la ciencia
En 1707 nace Carl von Linneo, el científico que cambió para siempre la forma en que entendemos la vida en la Tierra.
Gracias a él, hoy utilizamos la nomenclatura binómica, un sistema que permite nombrar y clasificar a todos los seres vivos con dos palabras: género y especie.
🌱 Homo sapiens
🌿 Escherichia coli
Puede parecer algo básico… pero sin este sistema, la ciencia moderna simplemente no podría funcionar como lo hace hoy.
🔬 ¿Por qué es tan importante en el mundo farma?
La clasificación precisa de organismos no solo es relevante para la biología, sino también para:
✔️ Identificación de microorganismos en laboratorio
✔️ Desarrollo de medicamentos
✔️ Control de calidad en procesos фарma
✔️ Investigación científica y reproducibilidad de resultados
En pocas palabras: ponerle nombre correcto a las cosas es el primer paso para generar conocimiento confiable.
🧠 Dato interesante:
Antes de Linneo, una misma especie podía tener múltiples nombres dependiendo del país o del científico. Su sistema trajo orden, estandarización y comunicación global en la ciencia.
Hoy, más de 300 años después, su legado sigue presente en cada laboratorio, cada análisis y cada avance científico.
Porque en ciencia —y especialmente en farma—
👉 el orden y la precisión lo son todo.
👇 ¿Ya conocías la historia detrás de cómo se nombran las especies?
👉 Si necesitas material conoce nuestro catálogo: https://bit.ly/4d838nV
Mujeres en la ciencia, la historia que casi no se cuenta
Publicado por [Tu nombre o el de tu blog] | 8 de marzo — Día Internacional de la Mujer
La historia de la ciencia está llena de descubrimientos que transformaron nuestro mundo. Pero no siempre el crédito llegó parejo. En este post repasamos la vida y aportes de cinco científicas cuyas contribuciones fueron decisivas, y —en muchos casos— invisibilizadas por sistemas académicos, prejuicios de género o dinámicas de poder. No se trata de “victimismo”, sino de entender la realidad histórica para corregirla hoy: reconocer el talento que fue silenciado es también una forma de abrir camino para las científicas del presente y del futuro.
Rosalind Franklin (1920–1958) — la foto que ayudó a revelar la vida
Rosalind Franklin fue una química y cristalógrafa inglesa especializada en difracción de rayos X. A comienzos de los años 50 obtuvo imágenes de la estructura del ADN —la famosa “Foto 51” es la más conocida— que revelaban la geometría helicoidal de la molécula. Esas imágenes fueron consultadas por James Watson y Francis Crick (que propusieron el modelo de doble hélice en 1953) y jugaron un papel clave en la confirmación del modelo. Franklin murió joven, en 1958, y en 1962 el Nobel de Fisiología o Medicina se otorgó a Watson, Crick y Maurice Wilkins; por entonces Franklin ya no estaba viva y su contribución fue, durante décadas, minimizada o tratada como secundaria. Con el paso del tiempo, historiadores y científicos reconocen que su trabajo experimental fue central para el descubrimiento del ADN.
Legado: rigor experimental y la urgencia de clarificar autorías y créditos en publicaciones científicas.
Lise Meitner (1878–1968) — la física que explicó la fisión nuclear
Lise Meitner, física austro-sueca de formación vienesa, trabajó durante años con el químico Otto Hahn. Tras los experimentos que detectaron fragmentación de núcleos pesados, Meitner, junto con su sobrino Otto Frisch, interpretó teóricamente el fenómeno como “fisión nuclear” (1938) y explicó la enorme liberación de energía asociada. Otto Hahn recibió el Nobel de Química (1944) por el descubrimiento experimental; Meitner fue ignorada en la concesión, en parte por su situación personal (era judía y tuvo que exiliarse) y en parte por las estructuras de reconocimiento de la época.
Legado: la importancia de la interpretación teórica y la ética científica en tiempos de conflicto; también un recordatorio de cómo factores sociales (género, etnia, guerra) moldean quién recibe el premio y la visibilidad.
Jocelyn Bell Burnell (n. 1943) — la estudiante que escuchó las estrellas
En 1967, como estudiante de posgrado en radioastronomía, Jocelyn Bell Burnell detectó señales regulares y extrañas en las gráficas de una antena: eran pulsos cortos y periódicos. Aquello llevó al descubrimiento de los púlsares (estrellas de neutrones emisoras de pulsos regulares). El Nobel de Física relacionado con ese hallazgo fue otorgado en 1974 a Antony Hewish (su supervisor) y Martin Ryle; Bell Burnell no fue incluida, aunque su trabajo de observación y análisis fue el origen del descubrimiento. Años después, la comunidad científica ha reconocido de múltiples maneras su papel crítico —y ella misma ha formado a generaciones de astrónomos.
Legado: la atención al detalle experimental y la contribución esencial de estudiantes y colaboradores en descubrimientos “de laboratorio”.
Chien-Shiung Wu (1912–1997) — la experta que comprobó un giro en las leyes físicas
Chien-Shiung Wu fue una física experimental china-estadounidense clave en la física de las partículas. En 1956 diseñó y ejecutó un experimento que demostró que la conservación de la paridad —una simetría asumida— no se cumple en interacciones débiles. Las predicciones teóricas que propusieron la posibilidad de esa violación (Lee y Yang) recibieron el Nobel de Física en 1957; Wu, cuya verificación experimental fue decisiva, no fue premiada. Su trabajo destacó por la precisión experimental y por abrir nuevas preguntas fundamentales sobre las simetrías en la naturaleza.
Legado: excelencia experimental y la necesidad de valorar por igual teoría y evidencia empírica.
Mary Anning (1799–1847) — la colectora que reconstruyó el pasado
Mary Anning fue una paleontóloga británica autodidacta, conocida por encontrar importantes fósiles marinos (como ictiosaurios y plesiosaurios) en las costas de Lyme Regis, Inglaterra. En una época en que las ciencias naturales estaban dominadas por hombres de clase alta, Anning —de origen modesto y mujer— vendía fósiles para subsistir y sin acceso pleno a las redes académicas que publicaban y acreditaban los hallazgos. Muchos de sus descubrimientos fueron descritos y publicados por científicos masculinos que sí obtuvieron reconocimiento académico.
Legado: la importancia del acceso equitativo a redes científicas y la justicia en la atribución del descubrimiento.
¿Qué nos enseñan estas historias?
- Las estructuras cuentan. No siempre es falta de mérito lo que explica la invisibilización: a menudo influyen normas institucionales, redes sociales, roles de clase y género, e incluso situaciones políticas y de guerra.
- Créditos y autorías importan. La forma en que asignamos reconocimiento (autores en un paper, firmantes, premios) moldea la memoria científica y las carreras futuras.
- Reconocer no es solo reparar el pasado, es cambiar el presente. Contar estas historias ayuda a diseñar políticas —mentoría, transparencia en autorías, comités diversos— que eviten que el talento vuelva a quedar en la sombra.
Conclusión
Recordar a Rosalind Franklin, Lise Meitner, Jocelyn Bell Burnell, Chien-Shiung Wu y Mary Anning no es solo conmemorar víctimas de una injusticia histórica: es aprender a construir instituciones donde el mérito sea reconocido sin sesgos. En este #8M propongamos medidas concretas en nuestros equipos y universidades: políticas claras de autoría, comités de revisión con perspectiva de género, programas de mentoría y visibilidad activa para científicas jóvenes. Esa es la forma práctica de honrar su legado.
Día Internacional de la Mujer y la Niña en la Ciencia: científicas mexicanas que transformaron el laboratorio
Esther Orozco Orozco (1945– )
Bióloga que contribuyó al entendimiento de microorganismos patógenos y la respuesta celular.
Esther Orozco Orozco es una destacada científica mexicana nacida el 25 de abril de 1945, egresada del Instituto Politécnico Nacional como Bióloga, con estudios de posgrado en ciencias biomédicas. Su trayectoria científica se ha centrado en la biología celular y la parasitología, particularmente en el estudio de Entamoeba histolytica, un parásito causante de amibiasis.
Desde la década de 1970 desarrolló investigación fundamental sobre los mecanismos de patogenicidad, adhesión celular y respuesta inmune frente a microorganismos, contribuyendo al entendimiento de cómo los patógenos interactúan con células huésped. Sus estudios aportaron bases experimentales para el control microbiológico, diagnóstico y prevención de enfermedades infecciosas, con implicaciones directas en salud pública y biotecnología.
Su trabajo fortaleció el conocimiento de procesos celulares críticos, esenciales para áreas como la microbiología clínica, la bioquímica de patógenos y la evaluación de riesgos biológicos en laboratorio.
Premios y reconocimientos profesionales:
- Investigadora Nacional Emérita del Sistema Nacional de Investigadores (SNI).
- Miembro de la Academia Mexicana de Ciencias.
- Diversos reconocimientos por su contribución a la ciencia biomédica en México.
Susana López Charretón (1957– )
Viróloga que transformó el entendimiento de la infección viral a nivel celular.
Susana López Charretón es una científica mexicana nacida el 22 de enero de 1957, egresada del Instituto Politécnico Nacional como Bióloga, con doctorado en Ciencias Biomédicas. Es reconocida internacionalmente por sus aportaciones a la virología molecular, en particular al estudio del rotavirus.
Desde su laboratorio en la UNAM, ha investigado los mecanismos de entrada, replicación y ensamblaje viral, así como la interacción virus–célula. Sus hallazgos permitieron comprender cómo ciertos virus atraviesan barreras celulares y cómo inducen respuestas específicas en el hospedero, conocimientos clave para el desarrollo de estrategias de control y prevención.
Su trabajo tiene impacto directo en cultivo celular, bioseguridad, control de contaminantes biológicos y validación de modelos experimentales, áreas críticas para laboratorios de investigación y control de calidad.
Premios y reconocimientos profesionales:
- Premio L’Oréal–UNESCO “La Mujer y la Ciencia”.
- Investigadora Nacional Emérita del SNI.
- Miembro de El Colegio Nacional.
María Elena Álvarez-Buylla Roces (1959– )
Bióloga molecular especializada en regulación genética y desarrollo celular.
María Elena Álvarez-Buylla es una científica mexicana nacida el 27 de marzo de 1959, bióloga por la UNAM y doctora en biología molecular. Su trabajo se ha enfocado en la regulación genética, redes de genes y desarrollo celular, utilizando modelos experimentales avanzados.
A lo largo de su carrera ha estudiado cómo los genes se activan y regulan en sistemas vivos, aportando bases fundamentales para la biología molecular moderna, la biotecnología y los bioprocesos. Sus investigaciones han contribuido a comprender la estabilidad genética y la expresión controlada de proteínas, aspectos esenciales para el desarrollo de productos biológicos seguros.
Estos conocimientos son clave para áreas como control de calidad, producción biotecnológica y evaluación de riesgos moleculares en laboratorio.
Premios y reconocimientos profesionales:
- Investigadora Nacional Emérita del SNI.
- Miembro de la Academia Mexicana de Ciencias.
- Reconocimientos internacionales en biología teórica y experimental.
Ana María Cetto Kramis (1946– )
Física con impacto directo en metrología, normalización y rigor científico.
Ana María Cetto es una científica mexicana nacida en 1946, doctora en física con una trayectoria destacada en metrología científica, normalización y política del conocimiento. Su trabajo se ha centrado en asegurar la calidad, trazabilidad y estandarización de las mediciones científicas.
Ha colaborado estrechamente con organismos internacionales en el desarrollo de criterios de evaluación, medición y validación científica, principios fundamentales para laboratorios analíticos, farmacéuticos y de control de calidad.
Su aportación es clave para entender la importancia de la medición confiable y reproducible, base de cualquier ensayo químico, biológico o bioquímico.
Premios y reconocimientos profesionales:
- Miembro de la Academia Mexicana de Ciencias.
- Participación destacada en organismos internacionales de ciencia y tecnología.
- Reconocimientos por su contribución a la cultura científica.
Rosaura Ruiz Gutiérrez (1950– )
Química que impulsó la ciencia aplicada y la formación científica en México.
Rosaura Ruiz Gutiérrez es una científica mexicana nacida en 1950, doctora en ciencias químicas por la UNAM. Su trayectoria combina la química, la educación científica y la gestión académica, con un fuerte énfasis en la ciencia aplicada.
Su trabajo ha contribuido a fortalecer la formación de profesionales en química y ciencias experimentales, promoviendo el uso riguroso del método científico y la integración del conocimiento químico en la industria y la investigación.
Su impacto se refleja en la consolidación de comunidades científicas y en la normalización de prácticas académicas que sostienen la investigación de laboratorio en México.
Premios y reconocimientos profesionales:
- Miembro de la Academia Mexicana de Ciencias.
- Reconocimientos por su labor académica y científica.
- Distinciones por su contribución a la educación superior.
Alejandra Bravo Mojica (1969– )
Microbióloga especializada en regulación genética bacteriana.
Alejandra Bravo Mojica es una científica mexicana nacida en 1969, bióloga por la UNAM y doctora en biología molecular. Su investigación se ha centrado en la regulación genética en bacterias, particularmente en Bacillus thuringiensis.
Ha estudiado cómo los genes bacterianos controlan la producción de proteínas, toxinas y mecanismos de supervivencia, aportando conocimiento fundamental para la microbiología molecular, biotecnología y control de microorganismos.
Estos estudios son relevantes para el entendimiento de procesos bacterianos, control de contaminantes y evaluación de riesgos biológicos en entornos industriales y de laboratorio.
Premios y reconocimientos profesionales:
- Investigadora Nacional Nivel III del SNI.
- Miembro de la Academia Mexicana de Ciencias.
- Reconocimientos internacionales en microbiología.
Irma Herrera Zúñiga (†)
Bioquímica enfocada en el análisis clínico y control de calidad.
Irma Herrera Zúñiga fue una científica mexicana dedicada a la bioquímica clínica y al desarrollo de métodos analíticos para el análisis de muestras biológicas. Su trabajo contribuyó a fortalecer la confiabilidad de pruebas bioquímicas utilizadas en diagnóstico y control de calidad.
Participó en la implementación y validación de procedimientos analíticos, enfatizando la importancia de la reproducibilidad, precisión y control de variables en laboratorio.
Su legado se refleja en la consolidación de prácticas analíticas rigurosas en el ámbito clínico y bioquímico.
Premios y reconocimientos profesionales:
- Reconocimientos académicos y profesionales en el área de bioquímica clínica.
- Aportaciones formativas en instituciones de educación superior.
Conclusión
El Día Internacional de la Mujer y la Niña en la Ciencia es un recordatorio de que el talento científico no tiene género y de que la curiosidad, la disciplina y la innovación son los verdaderos motores del conocimiento. Hoy, las mujeres están presentes en laboratorios, control de calidad, investigación y desarrollo, regulación, biotecnología, producción y muchas otras áreas que sostienen el avance científico y tecnológico.
En este recorrido presentamos solo una muestra de científicas mexicanas que, con rigor y compromiso, transformaron el trabajo de laboratorio y dejaron aportaciones que siguen vigentes. Su legado demuestra que la ciencia se construye con constancia, pensamiento crítico y pasión por comprender el mundo. Y quién sabe, quizá en el futuro el nombre que inspire a nuevas generaciones sea el tuyo y forme parte de nuestro próximo artículo.
Referencias – Formato APA simplificado
Esther Orozco Orozco
Instituto Politécnico Nacional. (s. f.). Trayectoria académica y científica de Esther Orozco Orozco. IPN.
Sistema Nacional de Investigadores. (s. f.). Investigadores nacionales eméritos. CONAHCYT.
Academia Mexicana de Ciencias. (s. f.). Miembros de la Academia Mexicana de Ciencias. AMC.
Susana López Charretón
Universidad Nacional Autónoma de México. (s. f.). Perfil académico de Susana López Charretón. Instituto de Biotecnología, UNAM.
El Colegio Nacional. (s. f.). Susana López Charretón, miembro de El Colegio Nacional. El Colegio Nacional.
UNESCO. (s. f.). Premio L’Oréal–UNESCO “La Mujer y la Ciencia”. UNESCO.
María Elena Álvarez-Buylla Roces
Universidad Nacional Autónoma de México. (s. f.). Perfil académico de María Elena Álvarez-Buylla Roces. Instituto de Ecología, UNAM.
Sistema Nacional de Investigadores. (s. f.). Investigadores nacionales eméritos. CONAHCYT.
Academia Mexicana de Ciencias. (s. f.). Miembros de la Academia Mexicana de Ciencias. AMC.
Ana María Cetto Kramis
Universidad Nacional Autónoma de México. (s. f.). Perfil académico de Ana María Cetto. Instituto de Física, UNAM.
International Atomic Energy Agency. (s. f.). Scientific advisory activities. IAEA.
Academia Mexicana de Ciencias. (s. f.). Miembros de la Academia Mexicana de Ciencias. AMC.
Rosaura Ruiz Gutiérrez
Universidad Nacional Autónoma de México. (s. f.). Trayectoria académica de Rosaura Ruiz Gutiérrez. Facultad de Ciencias, UNAM.
Academia Mexicana de Ciencias. (s. f.). Miembros de la Academia Mexicana de Ciencias. AMC.
Alejandra Bravo Mojica
Universidad Nacional Autónoma de México. (s. f.). Perfil académico de Alejandra Bravo Mojica. Instituto de Biotecnología, UNAM.
Sistema Nacional de Investigadores. (s. f.). Investigadores nacionales nivel III. CONAHCYT.
Academia Mexicana de Ciencias. (s. f.). Miembros de la Academia Mexicana de Ciencias. AMC.
Irma Herrera Zúñiga
Instituciones de educación superior en México. (s. f.). Materiales académicos y aportaciones en bioquímica clínica.
Asociaciones profesionales de análisis clínicos. (s. f.). Reconocimientos y contribuciones profesionales.
Biotecnología farmacéutica: avances en proteínas recombinantes y terapias génicas
La revolución silenciosa que está transformando la medicina moderna
La biotecnología farmacéutica vive una etapa histórica. Por primera vez en más de un siglo, la medicina se está alejando del enfoque tradicional —tratar síntomas— y se está moviendo hacia la corrección molecular de las causas de las enfermedades. Este cambio no es casual ni repentino; es el resultado de décadas de avances en ingeniería genética, bioinformática, purificación de biomoléculas y análisis estructural.
Entre los campos con mayor impacto destacan las proteínas recombinantes y las terapias génicas. Uno permite producir biomoléculas terapéuticas con una precisión casi quirúrgica; el otro reescribe las instrucciones defectuosas del propio cuerpo. Ambos representan la frontera de la medicina, y juntos están redefiniendo cómo entendemos la salud, la enfermedad y la posibilidad de curar lo hasta ahora incurable.
1. El origen de una revolución: de la ingeniería genética a la medicina personalizada
Para entender la magnitud de los avances actuales, conviene recordar que la medicina basada en moléculas recombinantes tiene apenas 40 años. Antes de 1982, una persona con diabetes dependía de insulina extraída de páncreas de cerdo o vaca. La diferencia estructural respecto a la insulina humana generaba reacciones adversas, baja disponibilidad y altos costos.
Todo cambió cuando se logró insertar el gen humano de la insulina en E. coli. Ese hecho —aparentemente simple— desató un paradigma completamente nuevo: si podemos “programar” células para producir proteínas humanas, también podemos programarlas para producir anticuerpos, enzimas, factores de coagulación o moléculas diseñadas a la medida.
Ese es el núcleo de la biotecnología farmacéutica actual:
- Comprender los genes.
- Manipularlos.
- Expresarlos en sistemas controlados.
- Convertirlos en terapias seguras y efectivas.
Hoy existen más de 350 productos biotecnológicos aprobados globalmente, y miles más en investigación. Entre ellos destacan proteínas recombinantes ultramodificadas, anticuerpos biosintéticos, vectores virales de nueva generación y terapias génicas capaces de corregir enfermedades devastadoras.
2. Proteínas recombinantes: ingeniería molecular con precisión terapéutica
Las proteínas recombinantes son, en esencia, proteínas de origen humano creadas en sistemas biológicos modificados. Lo sorprendente es la precisión con la que hoy se pueden diseñar.
2.1. Cómo se producen realmente
El proceso moderno combina varias disciplinas:
- Selección y diseño del gen
- Se elige la secuencia exacta que se desea expresar.
- Se optimiza para un organismo hospedero (codon optimization).
- En muchos casos ya no se replican proteínas naturales, sino versiones “mejoradas”.
- Inserción del gen en una línea celular
- E. coli para proteínas sencillas.
- Levaduras como Pichia pastoris para producir a gran escala.
- Células CHO para proteínas complejas como anticuerpos monoclonales.
- Cultivo en biorreactores
- Control estricto de pH, oxígeno, temperatura y nutrientes.
- Monitoreo en tiempo real mediante sensores ópticos, Raman y algoritmos predictivos.
- Purificación avanzada
- Cromatografía de afinidad (por ejemplo, captura por proteína A).
- Ultrafiltración, filtración estéril y validación microbiológica.
- Análisis estructural y funcional
- Espectrometría de masas para verificar integridad.
- Ensayos funcionales para asegurar actividad biológica.
Cada una de estas etapas se ha vuelto más rápida, más precisa y más automatizada.
2.2. La evolución de las proteínas recombinantes
Las proteínas recombinantes ya no se diseñan solo para “copiar” la naturaleza. Ahora se optimizan:
- Glicosilación dirigida para mejorar estabilidad.
- Mutagénesis dirigida para aumentar afinidad.
- Ingeniería de dominios para modificar vida media.
Ejemplos modernos incluyen:
- Insulinas de acción ultrarrápida optimizadas para pacientes con diabetes tipo 1.
- Factores de coagulación de vida media extendida que reducen drásticamente la frecuencia de inyecciones en hemofilia.
- Interferones y hormonas optimizadas para mayor solubilidad y menor inmunogenicidad.
Hoy, un anticuerpo monoclonal puede contener más de 1,300 modificaciones racionales, todas comprobadas experimentalmente para maximizar su seguridad y eficacia.
3. Terapias génicas: reparar la raíz del problema
Si las proteínas recombinantes actúan como “herramientas moleculares”, las terapias génicas actúan como arquitectos: no reparan la casa, reconstruyen los planos.
El objetivo de la terapia génica es simple en teoría:
Insertar, reemplazar o corregir genes para curar enfermedades.
En la práctica, es una hazaña tecnológica increíble.
3.1. Vectores virales: mensajeros de precisión
Los vectores virales modernos están diseñados para entregar material genético sin causar infección. Entre los más importantes destacan:
- AAV (virus adenoasociados)
Son los más seguros y ya se usan para tratar distrofia muscular, hemofilia y ceguera genética.
- Lentivirus
Se integran en el genoma. Se utilizan para CAR-T, terapias inmunológicas y correcciones permanentes.
- Adenovirus modificados
Entregan cargas más grandes, ideales para tejidos de alto recambio.
Cada vector es evaluado por:
- Tropismo (qué células infecta).
- Capacidad de carga genética.
- Seguridad e integración.
- Persistencia de expresión.
Hoy, gracias a ingeniería molecular avanzada, es posible dirigir vectores solo a hígado, músculo, neuronas o células hematopoyéticas con una exactitud sorprendente.
3.2. Edición genética: CRISPR y más allá
CRISPR ha sido el motor de la segunda ola de terapias génicas. La generación inicial cortaba ADN; la nueva edición es de precisión atómica:
- Base editing: cambia una sola letra del ADN sin cortarlo.
- Prime editing: reescribe secuencias completas.
- CRISPRi y CRISPRa: regulan genes sin modificarlos.
Esto permite corregir mutaciones puntuales en enfermedades como anemia falciforme, fibrosis quística o distrofias musculares.
3.3. Terapias aprobadas y resultados clínicos
En los últimos 5 años se aprobaron terapias que hace una década parecían ciencia ficción:
- Zolgensma: reemplazo de un gen completo para la atrofia muscular espinal.
- Luxturna: reversión de ceguera congénita causada por mutación RPE65.
- CAR-T comerciales: curación completa en ciertos pacientes con leucemia refractaria.
- Terapias génicas para hemofilia A y B: una sola administración sustituye años de plasma o factores recombinantes.
Estamos ante una medicina que promete terapias únicas, administradas solo una vez, con efectos potencialmente permanentes.
4. Retos actuales: seguridad, costo y escalabilidad
El avance es enorme, pero no exento de desafíos.
4.1. Seguridad
Aun con vectores optimizados, persisten riesgos:
- Respuesta inmune contra el vector.
- Integración genética no deseada.
- Expresión excesiva o insuficiente del gen terapéutico.
Los ensayos clínicos actuales incluyen análisis de toxicidad, biodistribución, inmunogenicidad y estudios genómicos de integración.
4.2. Producción a gran escala
Producir terapias génicas y recombinantes no es como fabricar un fármaco químico. Requiere:
- Biorreactores especializados.
- Medios libres de suero.
- Cell lines hiperespecializadas.
- Monitorización completa de microbiología, endotoxinas, ADN residual, etc.
Esto explica los costos actuales, aunque están disminuyendo conforme mejora la tecnología.
4.3. Accesibilidad
Las terapias génicas pioneras cuestan cientos de miles o millones de dólares.
Sin embargo, la historia se repite: así era con las terapias monoclonales hace 30 años.
Hoy son comunes y cada vez más accesibles.
La industria espera que los precios bajen entre 70% y 90% en la próxima década conforme aumentan la competencia, la automatización y los estándares globales.
5. El futuro: medicina regenerativa, proteínas “inteligentes” y edición en el cuerpo humano
La biotecnología farmacéutica está entrando en una fase nueva y fascinante.
5.1. Proteínas inteligentes
Próximamente veremos terapias diseñadas con comportamientos dinámicos:
- Anticuerpos que se activan solo en presencia de biomarcadores tumorales.
- Enzimas que cambian de conformación para modular su actividad según pH o temperatura.
- Proteínas sintéticas que nunca han existido en la naturaleza.
5.2. Terapia génica in vivo ultradirigida
Nuevos vectores permitirán editar genes directamente en:
- Cerebro
- Corazón
- Pulmones
- Riñón
Con una eficiencia que antes era imposible.
5.3. Ingeniería de células completas
CAR-T ya inició la tendencia, pero se extiende a:
- Macrófagos programados para combatir fibrosis.
- Células beta pancreáticas derivadas de iPS para revertir diabetes.
- Neuronas generadas en laboratorio para reemplazar áreas dañadas por Parkinson.
6. Conclusión: una medicina que repara en vez de tratar
La historia de la medicina está llena de momentos decisivos: la penicilina, las vacunas, los anticuerpos monoclonales.
La biotecnología farmacéutica —especialmente las proteínas recombinantes y las terapias génicas— es el siguiente gran salto.
Por primera vez, tenemos la capacidad de corregir, no solo aliviar.
De restaurar funciones, no solo retrasar deterioros.
De transformar el futuro de pacientes que hace pocos años no tenían ninguna alternativa terapéutica.
Estamos presenciando el nacimiento de una medicina verdaderamente personalizada y biológica. Una medicina que entiende que el cuerpo no solo puede enfermar: también puede aprender a repararse.
Bibliografía
- Walsh G. Biopharmaceuticals: Biochemistry and Biotechnology. Wiley; 2018.
- Mullard A. “Gene therapy clinical trials surge.” Nature Reviews Drug Discovery. 2023.
- High KA, Roncarolo MG. “Gene therapy.” New England Journal of Medicine. 2019.
- Ledford H. “CRISPR medicine enters the clinic.” Nature. 2020.
- Thomas CE, Ehrhardt A, Kay MA. “Progress and problems with the use of viral vectors for gene therapy.” Nature Reviews Genetics. 2003.
- Dunbar CE et al. “Gene therapy comes of age.” Science. 2018.
- Rosenberg SA, Restifo NP. “Adoptive cell transfer as personalized immunotherapy.” Science. 2015.
La Ciencia Nunca Descansa: Descubrimientos que Nacieron en Diciembre
Mientras el mundo se llena de luces, villancicos y aroma a ponche, los científicos del pasado seguían en sus laboratorios, probando, midiendo y anotando resultados…
Sí, aunque cueste creerlo, la ciencia no toma vacaciones —ni siquiera en Navidad.
Y es que, entre un brindis y otro, varios descubrimientos históricos sucedieron en diciembre, demostrando que la curiosidad humana no conoce de calendario (ni de cenas familiares con pavo). 🍗
🧬 1. El descubrimiento del ADN… casi como regalo navideño
En diciembre de 1952, Rosalind Franklin tomó una de las fotografías más importantes de la ciencia: la famosa Fotografía 51.
Gracias a su trabajo con difracción de rayos X, Watson y Crick pudieron deducir la estructura del ADN meses después.
Mientras muchos preparaban sus decoraciones, ella preparaba la base de la biología moderna. 🎁
⚛️ 2. Marie y Pierre Curie: un diciembre lleno de radiación (del tipo bueno)
En diciembre de 1898, los Curie anunciaron oficialmente el descubrimiento del radio y el polonio.
Entre tubos, sales y un invierno helado, lograron aislar sustancias que cambiarían para siempre la física y la medicina.
Quién sabe… tal vez aquel laboratorio parisino olía más a química que a pavo, pero fue una Navidad brillante —literalmente. ✨
💡 3. La electricidad que encendió las luces navideñas
El inventor Thomas Edison presentó su primera bombilla práctica en diciembre de 1879.
Poco después, iluminó su laboratorio con un centenar de focos para demostrar su invento.
Sin saberlo, estaba inspirando las luces del árbol de Navidad que hoy todos conocemos. 🔌🎄
🌡️ 4. Max Planck y el nacimiento de la física cuántica
El 14 de diciembre de 1900, Max Planck presentó ante la Sociedad Física de Berlín su teoría sobre la cuantización de la energía.
Sin ese descubrimiento, hoy no tendríamos láseres, pantallas LED ni chips de computadora.
Mientras otros contaban los días para la cena de Navidad, Planck contaba cuantos cuantos cabían en la energía.
🧫 5. Alexander Fleming y su hongo salvador
Aunque el descubrimiento de la penicilina fue antes, en diciembre de 1945 Fleming recibió el Premio Nobel de Medicina junto con Florey y Chain.
Y sí, probablemente brindó con sidra en vez de champaña, celebrando que millones de vidas serían salvadas gracias a un simple moho. 🍾
🎁 6. Más que regalos, descubrimientos
Podríamos decir que diciembre es un mes generoso con la humanidad.
Desde descubrimientos químicos hasta avances en física, los laboratorios no cierran cuando llega la Navidad.
Porque mientras unos desempacan obsequios, otros abren la puerta al conocimiento.
🎅 Así se vive la ciencia en estas fechas en Metrix Laboratorios:
con curiosidad, pasión y una chispa de inspiración…
porque la ciencia, igual que la Navidad, nunca deja de sorprendernos.
Calaverita del Dr. Trix en Metrix Laboratorios
En Metrix Laboratorios un día ocurrió,
que la huesuda llegó y todo observó.
Con bata prestada y lentes al revés,
quería saber qué hacía el Dr. Trix esta vez.
Entre tubos, pipetas y espuma brillante,
la ciencia bailaba, ¡era todo un instante!
“¿Qué estudias, mi doc?”, la flaca preguntó,
“Una fórmula nueva… ¡que hasta a ti sorprendió!”
El Químico rió con humor contagioso,
“Si te quedas aquí, puede ser peligroso.
Esto no es brujería, ni pócima fatal,
¡es pura ciencia, nivel molecular!”
Pero la muerte terca quiso probar,
y el matraz con burbujas se puso a agitar.
Un humo rosado cubrió el lugar,
y la flaca empezó… ¡a resucitar!
Desde entonces ronda con bata y color,
dice que en Metrix encontró su labor.
Porque entre ciencia, humor y reacción,
hasta la muerte aprendió… ¡química con pasión! ⚗️💀
10 reglas de laboratorio que NUNCA debes hacer.
10 reglas de laboratorio que NUNCA debes hacer Por qué importa conocer estas reglas La seguridad en el laboratorio protege tu salud, la de tus compañeros y la validez de tus resultados. Conocer las reglas de laboratorio que no se deben hacer reduce accidentes, costes y problemas regulatorios. 1. No comer, beber ni aplicar cosméticos dentro del área de trabajo Riesgo: ingestión de contaminantes y contaminación cruzada. Consejo: establece una zona limpia fuera del laboratorio y prohíbe alimentos en el área. Ejemplo: guardar comida en una nevera compartida con reactivos químicos puede provocar ingestión accidental de trazas. 2. No
pipetear con la boca (nunca) Riesgo: exposición directa a agentes biológicos y químicos. Consejo: utiliza dispositivos mecánicos de
pipeteo siempre; reporta si faltan. Si observas a alguien
pipeteando con la boca, notifícalo al responsable y ofrece alternativas seguras. 3. No trabajar sin el equipo de protección personal (
EPP) adecuado Riesgo: quemaduras, proyecciones, exposición cutánea y ocular. Consejo: conoce qué guantes y gafas corresponden para cada sustancia; reemplázalos cuando estén comprometidos. No todos los guantes protegen frente a todos los solventes; verifica compatibilidad. 4. No usar reactivos sin leer la Hoja de Seguridad (
SDS) ni las etiquetas Riesgo: mezclas incompatibles, respuestas incorrectas en emergencias. Consejo: revisa
SDS antes de usar y etiqueta recipientes secundarios con nombre, concentración y fecha. Las
SDS contienen información sobre primeros auxilios, tiempo de exposición seguro y compatibilidades. 5. No almacenar alimentos junto a reactivos o muestras Riesgo: contaminación de alimentos y exposición. Consejo: usa neveras separadas y señala su uso en la política del laboratorio. Si no hay nevera separada, documenta la necesidad y solicita una política escrita. 6. No manipular cabinas o campanas sin formación ni verificación Riesgo: generación de aerosoles, recirculación de aire contaminado. Consejo: solicita certificación regular y verifica funcionamiento antes de trabajar. Asegúrate de que las cabinas tengan certificación vigente y filtros adecuados. 7. No improvisar en la gestión de residuos Riesgo: reacciones peligrosas, multas, exposición del personal de limpieza. Consejo: usa contenedores etiquetados y sigue la ruta de residuos de la institución. Nunca mezcles residuos incompatibles (por ejemplo oxidantes con orgánicos). 8. No trabajar solo en procedimientos de alto riesgo ni ignorar los
SOP Riesgo: ausencia de respuesta inmediata ante accidentes. Consejo: coordina un compañero y documenta cualquier desviación del
SOP. Para trabajos con irradiación, agentes infecciosos o solventes volátiles, pide supervisión y plan de emergencia. 9. No ocultar incidentes o
near-misses; repórtalos siempre Riesgo: repetición de errores y agravamiento de incidentes. Consejo: participa en la cultura de reporte; propón soluciones prácticas al reportar. Los
near-misses enseñan más que los accidentes graves si se documentan correctamente. 10. No confundir limpieza con descontaminación ni usar atajos Riesgo: agentes viables o residuos activos persistentes. Consejo: sigue las concentraciones y tiempos de contacto indicados; registra limpiezas en áreas críticas. Limpieza física no elimina necesariamente agentes biológicos; usa desinfectantes aprobados según el agente. ¿Cuántas cosas ya hiciste exponiéndote o a tus compañeros?
El laboratorio del agave: Donde México se vuelve ciencia.
Un recorrido 100% mexicano que une historia y ciencia
Beber tequila o mezcal es beber México: es beber campo, pueblo, oficio y paisaje. Pero detrás del rito que une paladar y fiesta —los vapores del alambique, el humo del horno, la piña cortada al amanecer— hay una historia larga y una ciencia precisa que permite conservar ese patrimonio sin renunciar a la seguridad ni a la identidad.
Este texto recorre, desde una mirada enteramente mexicana, cómo la tradición y la técnica han tejido juntos el carácter de nuestros destilados, y por qué la ciencia es hoy el mejor aliado para que el legado del agave siga intacto.
Del maguey a la memoria colectiva
El vínculo entre México y el agave es ancestral. Antes de la llegada de la destilación ya existía el pulque —fermentado del aguamiel— que pobló plazas y ceremonias. Más tarde, con la adopción del arte de destilar, surgieron los palenques y los alambiques en los que cada región imprimió su sello: en Oaxaca, el mezcal con su humo; en Jalisco, el tequila que se volvió símbolo nacional. Es una historia de adaptación: técnicas traídas y transformadas, saberes locales que aprendieron a dialogar con nuevas herramientas.
Ese patrimonio no es homogéneo: existen tantos mezcales como pueblos; tantos tequilas como familias en Jalisco. Cada botella contiene una geografía, un clima y una decisión artesanal. Y cada decisión —desde la selección de la piña hasta el tipo de horno— modela la química del producto final.
Ciencia mexicana al servicio de la tradición
Decir que un proceso es tradicional no significa que deba estar exento del escrutinio científico. La ciencia aporta dos cosas fundamentales: comprensión y protección. Comprensión, porque explica por qué un cocido en horno de piedra genera notas ahumadas distintas a una cocción al vapor; protección, porque permite detectar y corregir riesgos que amenacen la salud del consumidor o la reputación del productor.
En los laboratorios mexicanos y en los palenques, hoy se usan técnicas que antes parecían lejanas: cromatografía de gases para perfilar compuestos volátiles, análisis fisicoquímicos para medir alcoholes y acidez, y registros de trazabilidad que enlazan cada lote con la parcela que produjo la piña. Todo esto no homogeneiza el sabor: lo documenta y lo respalda.
Tradición y química: el baile de los compuestos
La magia sensorial del mezcal y el tequila se explica en el laboratorio. En la fermentación, microorganismos locales transforman azúcares en etanol, ácidos y aromas; en la destilación, las leyes físicas de volatilidad separan familias de compuestos que el maestro destilador, con oficio, convierte en cuerpo y bouquet. La química no roba misterio: lo hace legible.
Además, la ciencia identifica y mide aquello que no debería pasar: compuestos indeseados que pueden elevar riesgos si no se controlan. Por ejemplo, la presencia de ciertos alcoholes volátiles se monitorea y se gestiona para garantizar que la bebida celebre sin poner en riesgo a quien la consume. Esa vigilancia técnica es parte del respeto por la tradición: protegerla para que viaje segura a nuevas generaciones.
Regiones, manos y saberes: la diversidad como fortaleza
México es rico en agaves y en técnicas productivas. Cada región aporta una paleta sensorial: los agaves silvestres de Oaxaca, los paisajes volcánicos de Jalisco, los procesos y prácticas de Guerrero o Zacatecas. La ciencia permite mapear esa diversidad —químicamente y biológicamente— y convertirla en un activo: saber qué compuestos definen a un mezcal de tal palenque, o cómo una práctica local influye en la calidad final.
Esa cartografía del sabor y la técnica convierte al productor en guardián de la identidad. Y al consumidor, en participante informado de una tradición viva.
Celebrar septiembre con orgullo y conocimiento
En el mes patrio, cuando las plazas se llenan y los brindis se multiplican, celebrar con tequila y mezcal adquiere un significado extra: es un acto de memoria y de responsabilidad. La mejor manera de honrar ese patrimonio es consumir y producir con orgullo informado: reconocer las raíces, valorar las manos que trabajan y también exigir controles que protejan la salud pública y la reputación del oficio.
La ciencia en México no viene a reemplazar los saberes; los acompaña. Y es esa alianza —historia que nutre técnica, técnica que cuida tradición— la que hace posible que cada botella lleve, además de aroma y sabor, la garantía de un país que valora lo suyo.
Un compromiso mexicano
Un recorrido 100% mexicano que une historia y ciencia no es solo una frase: es un compromiso. Es la promesa de que cuidamos lo nuestro con orgullo y rigor. En septiembre —y todo el año—, celebrar con tequila y mezcal es celebrar una conversación entre manos y laboratorio, entre maestros destiladores y técnicos de control; es asegurar que la herencia del agave siga siendo nuestra, auténtica y segura.
Científicas invisibles
En la historia de la ciencia, abundan los nombres que definieron eras: Pasteur, Lister, Koch, Watson, Crick… Sin embargo, en esa narrativa lineal y predominantemente masculina, han quedado marginadas muchas de las mentes que hicieron posibles los descubrimientos que hoy sostienen nuestras prácticas de laboratorio.
Este artículo no pretende únicamente rendir homenaje, sino reconocer las contribuciones técnicas y metodológicas de científicas cuyos descubrimientos aún resuenan en los protocolos, reactivos y equipos que empleamos cada día en entornos de control microbiológico, histología, biotecnología y farmacología.
🔬 Fanny Hesse y el agar-agar: la base sólida de la microbiología
En 1881, mientras trabajaba junto a su esposo Walther Hesse, colaborador directo de Robert Koch, Fanny Angelina Hesse propuso una solución que transformaría para siempre el cultivo de microorganismos: reemplazar la gelatina —que se licuaba a temperaturas superiores a 28 °C y era degradable por muchas bacterias— por agar-agar, un polisacárido extraído de algas rojas.
Fanny conocía el agar por su uso culinario en la cocina malaya. Su propuesta fue tan simple como revolucionaria: un medio estable a 37 °C, transparente, no nutritivo para la mayoría de las bacterias, y con excelentes propiedades gelificantes. Koch adoptó la idea casi de inmediato en su laboratorio, y sin embargo, el crédito quedó históricamente registrado sólo a su alrededor.
Aplicaciones modernas
Más de 140 años después, el agar-agar sigue siendo el estándar oro para medios de cultivo sólidos. Desde el recuento de aerobios mesófilos en industria alimentaria, hasta el monitoreo de microorganismos viables en salas limpias (mediante placas RODAC, por ejemplo), el aporte de Hesse está presente en cada incubadora, cada estufa y cada técnica de conteo en superficie.
🧬 Rosalind Franklin: la estructura del ADN y la precisión del dato
Rosalind Franklin fue una cristalógrafa británica cuya habilidad para obtener imágenes de alta resolución mediante difracción de rayos X permitió visualizar, por primera vez, la estructura helicoidal del ADN. Su famosa “Fotografía 51”, obtenida en 1952, fue crucial para que Watson y Crick desarrollaran el modelo de doble hélice publicado en Nature en 1953.
Sin embargo, Franklin no fue informada de que sus datos habían sido compartidos sin su permiso, y su nombre no apareció como coautora. Murió en 1958, y el Nobel de Medicina fue otorgado a Watson, Crick y Wilkins en 1962, cuando los premios no se otorgaban póstumamente.
Impacto en la biotecnología moderna
Comprender la estructura del ADN es la base de prácticamente todo lo que hoy llamamos biotecnología molecular: desde PCR y secuenciación genética, hasta la producción recombinante de proteínas (como las alternativas modernas a las pruebas LAL, como el rFC). Sin los datos de Franklin, el modelo tridimensional del ADN hubiera tardado mucho más en desarrollarse.
En los laboratorios actuales, el trabajo de Franklin vive en cada ciclo de termociclador, en cada diseño de oligonucleótidos y en cada kit de amplificación genética.
🧫 Esther Lederberg: una mente detrás de la genética bacteriana
Esther Lederberg fue pionera en la genética bacteriana durante los años 50, una época en la que pocos creían que las bacterias podían intercambiar material genético de forma compleja. Su trabajo fue clave para demostrar la existencia de plásmidos y para desarrollar la técnica de réplica de placas (replica plating), una metodología esencial para identificar mutantes y estudiar resistencia antibiótica.
Además, descubrió el fago lambda, que se convirtió en modelo universal para el estudio de la transducción genética.
Técnica que sigue vigente
La técnica de réplica de placas es aún utilizada en laboratorios de microbiología industrial para:
- La selección de colonias resistentes a antibióticos o desinfectantes.
- El estudio de mutaciones inducidas por estrés.
- El aislamiento de cepas productoras de metabolitos de interés en fermentaciones industriales.
Esther aportó no sólo datos, sino técnicas experimentales reproducibles que se integraron a la cultura experimental bacteriana de los laboratorios.
💊 Gertrude Elion: ingeniería farmacológica antes del genoma
Gertrude Elion comenzó su carrera sin acceso a estudios de doctorado por ser mujer, pero logró trabajar en investigación para Burroughs Wellcome (hoy parte de GSK), donde lideró un enfoque nuevo: diseñar fármacos dirigidos contra rutas bioquímicas específicas de las células enfermas.
Desarrolló fármacos como:
- 6-mercaptopurina, contra leucemia.
- Aciclovir, uno de los primeros antivirales eficaces contra herpes.
- AZT, base del primer tratamiento eficaz contra VIH.
Ganó el Premio Nobel en 1988 junto con George Hitchings.
De lo empírico al diseño racional
El enfoque de Elion antecedió lo que hoy se conoce como medicina personalizada o diseño racional de fármacos. Su idea fue cambiar el paradigma: dejar de probar cientos de compuestos al azar, y comenzar a diseñar moléculas dirigidas a blancos terapéuticos específicos.
Este enfoque es esencial en laboratorios de I+D de medicamentos, y su influencia puede verse en cada modelo de docking molecular o diseño de inhibidores en la industria actual.
📌 Epílogo: del olvido al laboratorio
Estas científicas no sólo aportaron conocimiento. Desarrollaron herramientas, técnicas, enfoques, medios y criterios que estructuran nuestro trabajo diario en el laboratorio moderno. Desde la selección del medio de cultivo hasta la validación de biológicos recombinantes, pasando por la caracterización genética de cepas o la elección de métodos analíticos, sus legados son funcionales, no simbólicos.
En Metrix Laboratorios, como parte del ecosistema técnico que respalda procesos críticos en las industrias farmacéutica, alimentaria, cervecera y de dispositivos médicos, creemos que el reconocimiento no es únicamente un acto de justicia histórica, sino también un ejercicio de profesionalismo técnico. Reconocer las raíces de nuestras metodologías fortalece nuestro criterio, enriquece nuestras decisiones y mejora nuestros procesos.
¡Ojo alMicroscopio! La Historia de Marcello Malpighi.
Marcello Malpighi (Crevalcore, 1628 – Roma, 1694) es ampliamente considerado el fundador de la anatomía microscópica y padre de la histología. Médico y biólogo italiano, empleó el microscopio recientemente inventado para examinar tejidos vivos, descubriendo estructuras que antes eran invisibles. Durante casi cuarenta años Malpighi utilizó el microscopio sistemáticamente para describir los tipos principales de estructuras en plantas y animales, sentando las bases de la histología moderna.
Biografía y formación
Malpighi nació en Crevalcore, cerca de Bolonia, en 1628. Estudió Medicina y Filosofía en la Universidad de Bolonia, donde obtuvo su doctorado en 1653. En 1656 fue nombrado profesor de medicina teórica en la Universidad de Pisa, donde inició sus observaciones microscópicas y comenzó a cuestionar críticamente las teorías tradicionales de Galeno y otros clásicos. Posteriormente regresó a Bolonia (1660) y ejerció allí la medicina práctica durante 25 años. Entre 1662 y 1666 ocupó la cátedra de medicina en Messina, y en 1691 fue llamado a Roma como médico personal del papa Inocencio XII. Falleció en Roma en 1694.
Descubrimientos fundamentales en histología
Los hallazgos de Malpighi revolucionaron la biología y la medicina de su época. Entre sus contribuciones más destacadas se encuentran:
- Pulmón: en 1661 describió la red de capilares pulmonares que conecta arterias y venas en los alvéolos, confirmando experimentalmente la circulación sanguínea propuesta por William Harvey
- Riñón y bazo: examinó meticulosamente la estructura del riñón y el bazo, identificando el corpúsculo renal (glomérulo) y los folículos esplénicos que hoy llevan el nombre de Malpighi.
- Sangre: fue el primero en observar los glóbulos rojos bajo el microscopio y atribuirles el color de la sangre.
- Piel y papilas: describió la capa más profunda de la epidermis (actual capa basal o estrato de Malpighi) y las papilas linguales responsables del gusto.
- Embriología e insectos: detalló por primera vez el desarrollo del embrión de pollo y estudió la anatomía del gusano de seda (silkworm), identificando órganos como las glándulas productoras de seda y el ovipositor.
- Respiración de insectos: descubrió que los insectos respiran por tráqueas (agujeros en la piel), adelantándose en siglos a la fisiología moderna.
Estos descubrimientos desterraron creencias médicas antiguas y abrieron el camino a la histología y la fisiología modernas. Muchas estructuras microscópicas en humanos y animales (corpúsculos de Malpighi, túbulos renales, Malpighian bodies, etc.) llevan su nombre en reconocimiento a sus aportes.
Métodos innovadores
Para obtener estos resultados, Malpighi innovó en la preparación de tejidos al microscopio. Implementó técnicas de fijación tempranas —como el uso de tintes rudimentarios e inyecciones de cera— para preservar y visualizar partes muy finas de los órganos. Con frecuencia comparó al animal estudiado con un “microscopio de la naturaleza” porque los tejidos de una rana o un gusano servían de lente natural que revelaba estructuras ocultas a simple vista. Aunque muchas de sus interpretaciones iniciales (por ejemplo, la idea de diminutas “glándulas” en los tejidos) fueron luego corregidas, Malpighi preparó el terreno para la teoría celular y la histología.
En suma, la obra de Malpighi estableció un enfoque experimental y observacional que inspira a los histólogos actuales: su rigor en el estudio microscópico, su espíritu crítico frente a la tradición y su curiosidad por diversos modelos biológicos (plantas, insectos, embriones) son aún hoy ejemplo de metodología científica avanzada.
Impacto en la ciencia médica y la microscopía moderna
Los fundamentos establecidos por Malpighi tienen eco en la medicina contemporánea. Por primera vez se correlacionaron las estructuras microscópicas con funciones fisiológicas —p. ej. los eritrocitos en el transporte de oxígeno— lo que permitió avances posteriores en fisiología y patología. Sus descripciones obligaron a replantear teorías clásicas y facilitaron la creación del diagnóstico histopatológico basado en cortes y tinciones. En la era actual, el microscopio óptico y las técnicas de histología son herederos directos de aquellos pioneros experimentos, con equipos cada vez más precisos que refinan la observación iniciada por Malpighi. Su legado multidisciplinario incentiva a los histólogos a integrar conocimientos (biología, química, tecnología de preparación) para mejorar continuamente el estudio de los tejidos.
De descubrimientos clásicos a herramientas modernas
La siguiente tabla compara algunos hitos históricos de la histología con las herramientas actuales del laboratorio:
| Técnica clásica | Herramienta actual en histología moderna |
| Aplicación de tinciones primitivas (ej. carmín de Hill en el s. XVIII) | Portaobjetos de vidrio de alta calidad para montajes y tinciones histológicas |
| Inclusión en parafina de muestras (s. XIX) | Moldes para inclusión de tejidos en parafina |
| Conservación criogénica básica de muestras | Cajas criogénicas y criotubos para almacenamiento en frío seguro |
Estas equivalencias ilustran cómo métodos pioneros (tinciones, parafina, criogenia) se complementan hoy con equipos estandarizados de laboratorio. Por ejemplo, el cuidado en la preparción de cortes histológicos clásico requiere ahora portaobjetos de cristal de precisión, y la inclusión en parafina utiliza moldes especializados. La conservación de muestras a bajas temperaturas, antes experimentada de modo rudimentario, se realiza hoy en criocajas diseñadas para estantes de congelación.
En la práctica actual, contar con insumos de calidad facilita enormemente estas tareas histológicas. Productos como criocajas, moldes de inclusión ————– ofrecen alta confiabilidad en la preparación de muestras. Simport es una marca reconocida que provee dichos suministros con altos estándares de calidad, adaptados a las exigencias modernas del laboratorio. Metrix, distribuidor oficial de Simport, es una fuente confiable para obtener estos materiales especializados, en conjunto, el ejemplo de Malpighi recuerda que el avance científico requiere tanto visión de futuro como herramientas adecuadas. Su legado inspira a los profesionales de histología de hoy: estudiar más allá de lo visible, innovar en técnicas y apoyarse en equipamiento de precisión son las claves que persisten desde sus días hasta la labor actual en el microscopio.
Página siguiente »